در شیمی دارویی، درک رفتار داروها در محیطهای مختلف بدن بدون توجه به یونیزاسیون و pKa عملاً ناقص خواهد بود. بسیاری از داروها بهصورت اسیدهای ضعیف یا بازهای ضعیف هستند و میزان یونیزه یا غیریونیزه بودن آنها به pH محیط بستگی دارد. این ویژگی مستقیماً بر لیپوفیلیسیته، عبور از غشاهای زیستی و در نهایت جذب دارو اثر میگذارد.
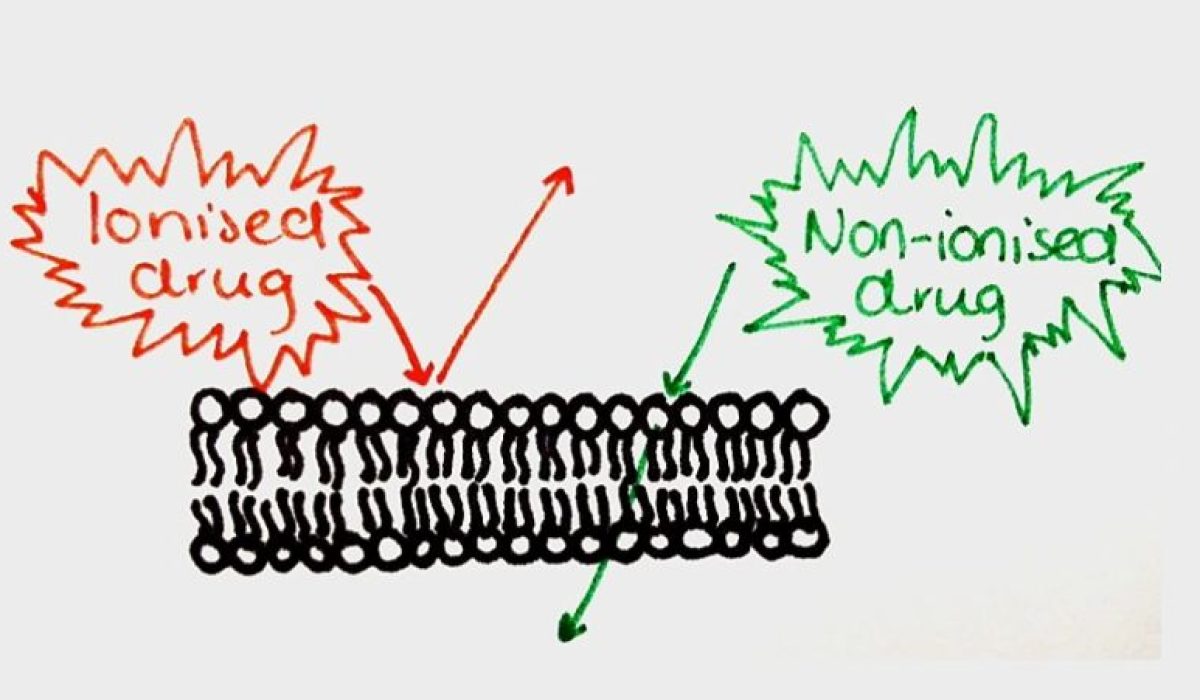
اصل کلی این است که فرم غیریونیزه دارو به دلیل قطبیت کمتر، راحتتر از غشای لیپیدی سلولها عبور میکند، در حالی که فرم یونیزه معمولاً در محیطهای آبی باقی میماند. به همین دلیل، محل جذب دارو در دستگاه گوارش یا بافتهای دیگر به تعادل میان pKa دارو و pH محیط وابسته است.
اسیدهای ضعیف، بازهای ضعیف و رفتار آنها در بدن
اسیدهای ضعیف در محیطهای اسیدی تمایل دارند به شکل غیریونیزه (HA) باقی بمانند، در حالی که در محیطهای قلیاییتر به فرم یونیزه (A⁻) تبدیل میشوند. در مقابل، بازهای ضعیف در محیطهای اسیدی بیشتر بهصورت یونیزه (BH⁺) وجود دارند و با افزایش pH، سهم فرم غیریونیزه آنها افزایش مییابد.
این تفاوت ظاهراً ساده، نقش بسیار مهمی در محل جذب، سرعت جذب و حتی توزیع دارو در بدن ایفا میکند و مبنای بسیاری از تصمیمات فارماکوکینتیکی و بالینی است.
آسپرین بهعنوان نمونهای از یک اسید ضعیف
آسپرین یا Acetylsalicylic acid یک اسید ضعیف با pKa حدود 3.5 است. در محیط بسیار اسیدی معده با pH حدود 1 تا 2، بخش عمدهای از آسپرین بهصورت غیریونیزه (HA) قرار دارد. این فرم، لیپوفیلتر است و بهراحتی میتواند از غشای سلولی اپیتلیوم معده عبور کند. به همین دلیل، جذب اولیه آسپرین در معده امکانپذیر و تسهیل میشود.
پس از ورود آسپرین به روده و سپس پلاسما که pH آن حدود 7.4 است، تعادل به سمت فرم یونیزه (A⁻) جابهجا میشود. یونیزه شدن دارو در این محیط باعث کاهش بازگشت آن به معده و ایجاد پدیدهای به نام ion trapping میگردد. این مکانیسم موجب افزایش ماندگاری آسپرین در گردش خون و تقویت اثر سیستمیک آن میشود و نمونهای روشن از ارتباط مستقیم pKa، pH و توزیع دارو در بدن است.
لیدوکائین بهعنوان نمونهای از یک باز ضعیف
لیدوکائین یک باز ضعیف با pKa حدود 7.9 است که رفتار آن در بدن تفاوت قابلتوجهی با آسپرین دارد. در محیط اسیدی معده، لیدوکائین تقریباً بهطور کامل در فرم یونیزه قرار میگیرد و در نتیجه جذب خوراکی آن در این ناحیه بسیار ناچیز است. با ورود دارو به روده باریک، pH محیط به pKa نزدیکتر میشود و بخش قابلتوجهی از لیدوکائین به فرم غیریونیزه درمیآید.
با وجود این، هرچند جذب لیدوکائین از روده به دلیل سطح جذب بالا و خونرسانی مناسب انجام میشود، اما دارو بلافاصله وارد کبد شده و دچار متابولیسم عبور اول شدید میگردد. در نتیجه، مقدار مؤثری از دارو به گردش خون سیستمیک و محل اثر خود نمیرسد و به همین دلیل مصرف خوراکی لیدوکائین کاربرد بالینی ندارد.
در مقابل، هنگام مصرف موضعی یا تزریقی، دارو مستقیماً به بافت هدف میرسد. در اطراف نورونها، فرم غیریونیزه لیدوکائین از غشای عصبی عبور میکند و سپس با یونیزه شدن در داخل سلول، به کانالهای سدیمی وابسته به ولتاژ متصل میشود. این اتصال منجر به مهار هدایت عصبی و ایجاد اثر بیحسی موضعی میگردد و نمونهای دقیق از نقش دوگانه یونیزاسیون در عبور غشایی و اثر فارماکودینامیک دارو است.
جمعبندی
یونیزاسیون و pKa از مفاهیم بنیادی شیمی دارویی هستند که درک آنها برای تحلیل جذب، توزیع و اثر داروها ضروری است. مثالهایی مانند آسپرین و لیدوکائین نشان میدهند که محل جذب دارو، فرم مصرف و حتی کاربرد بالینی آن تا چه حد به تعادل میان pH محیط و pKa دارو وابسته است. شناخت این اصول به داروسازان و متخصصان علوم پزشکی کمک میکند تا رفتار داروها را بهتر پیشبینی کرده و تصمیمات درمانی دقیقتری اتخاذ کنند.