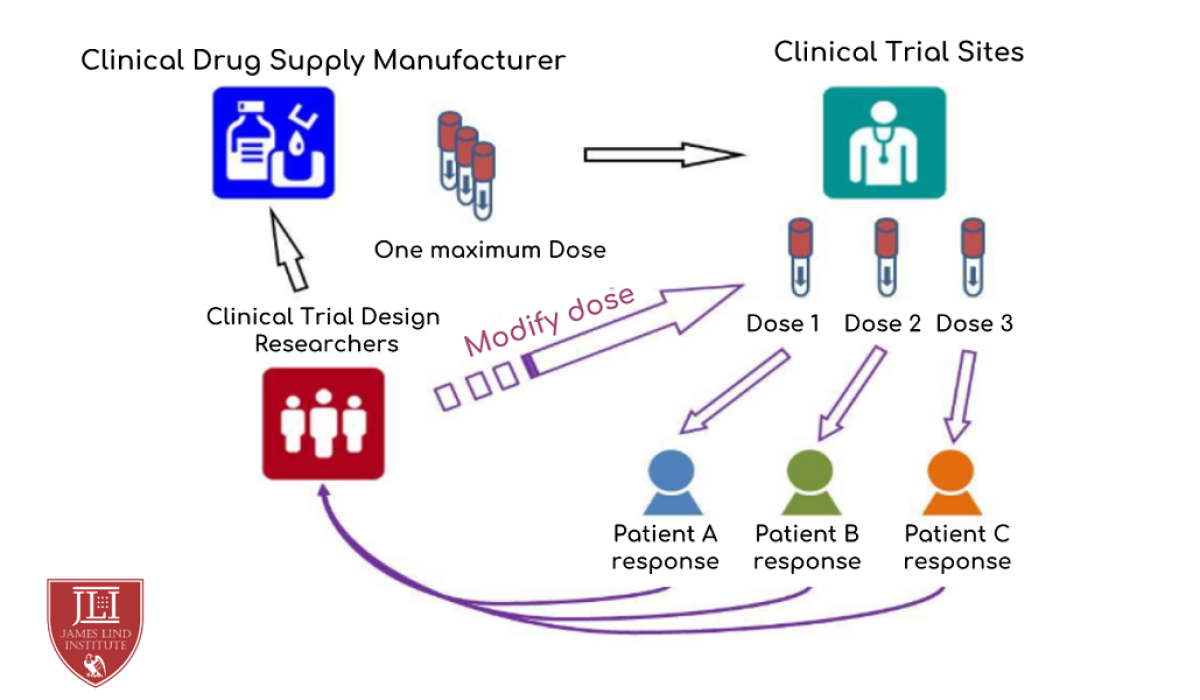
با پیچیدهتر شدن فرآیند توسعه دارو، نیاز به انعطافپذیری بیشتر در طراحی مطالعات بالینی بیش از گذشته احساس میشود. طراحی تطبیقی (Adaptive Design) پاسخی است به این نیاز که به محققان اجازه میدهد در حین اجرای مطالعه و بر اساس تحلیل دادههای میانی، ساختار مطالعه را بهینه کنند. در این مقاله، با مهمترین انواع طراحیهای تطبیقی در مطالعات دارویی آشنا میشویم و کاربرد هرکدام را بررسی میکنیم.
1. طراحی تطبیقی برای تعیین دوز بهینه (Adaptive Dose-Finding Design)
این نوع طراحی، عمدتاً در مطالعات فاز I و اوایل فاز II استفاده میشود و هدف آن یافتن دوزی است که بیشترین اثربخشی را با کمترین عوارض جانبی داشته باشد.
روشهای رایج:
- 3+3 Design (روش سنتی)
- Continual Reassessment Method (CRM): الگوریتمی برای بروزرسانی تخمین دوز بر اساس پاسخ بیماران
- Bayesian Optimal Interval Design: استفاده از تحلیل بیزین برای اصلاح محدوده دوز
کاربرد:
- در مطالعات داروهای شیمیدرمانی یا ایمونوتراپی
- در داروهایی با Window درمانی باریک (narrow therapeutic window)
2. طراحی تطبیقی با تصادفیسازی پاسخمحور
(Response-Adaptive Randomization)
در این طراحی، احتمال تخصیص بیماران به یک بازوی درمانی بهصورت پویا و در پاسخ به نتایج اولیه تغییر میکند. بهعبارت سادهتر، بیماران آینده بیشتر به درمانهایی اختصاص داده میشوند که بهتر عمل کردهاند.
کاربرد:
- در مطالعاتی که بازوهای درمانی متعددی دارند
- برای بهینهسازی تخصیص بیماران و افزایش شانس دریافت درمان مؤثر
مزایا:
- کاهش ریسک قرارگیری در بازوهای بیاثر
- افزایش کارایی و پاسخگویی سریعتر به اثربخشی درمانها
3. طراحی تطبیقی با بازنگری حجم نمونه
(Sample Size Re-estimation Design)
در این طراحی، حجم نمونه مطالعه در طول مسیر میتواند افزایش یا کاهش یابد تا اطمینان حاصل شود که توان آماری مطالعه (statistical power) کافی خواهد بود.
روشها:
- Blinded Sample Size Re-estimation: بدون اطلاع از گروه درمان
- Unblinded Sample Size Re-estimation: با تحلیل اثر درمان و انحراف معیار واقعی
کاربرد:
- زمانی که تخمینهای اولیه از انحراف معیار یا اثر درمان نامطمئن باشند
- برای جلوگیری از underpower یا overenrollment
4. طراحی حذف بازوهای ناکارآمد
(Drop-the-Loser Design)
اگر در تحلیلهای میاندورهای مشخص شود که یک یا چند بازوی درمانی عملکرد ضعیفی دارند، آن بازوها حذف میشوند و مطالعه با بازوهای باقیمانده ادامه مییابد.
کاربرد:
- مطالعات چند بازویی فاز II
- غربالگری اولیه چند دارو یا دوز
مزایا:
- صرفهجویی در منابع
- تمرکز بیشتر بر درمانهای امیدبخش
5. طراحی پیوسته فاز II/III
(Seamless Phase II/III Design)
در این نوع طراحی، فاز دوم و سوم مطالعه بهصورت یکپارچه انجام میشوند. در فاز اول اثربخشی اولیه بررسی میشود و در صورت اثبات، بدون توقف مطالعه، مستقیماً وارد فاز III میشوند.
کاربرد:
- در مطالعات تسریعشده (Accelerated Development Programs)
- برای کاهش زمان کلی توسعه دارو
مزایا:
- حذف زمان توقف بین فازها
- استفاده مجدد از دادههای فاز دوم در تحلیل نهایی
6. طراحی تطبیقی با تغییر نقطه پایانی (Endpoint Adaptation)
گاهی در حین مطالعه مشخص میشود که نقطه پایانی اولیه (مانند کاهش فشار خون) به اندازه کافی حساس نیست. در این حالت، نقطه پایانی مطالعه میتواند تغییر کند، البته به شرط آنکه در پروتکل پیشبینی شده باشد.
7. طراحی چندمرحلهای با توقف زودهنگام
(Group Sequential Design)
در این طراحی، تحلیلهای متوالی برای بررسی امکان توقف زودهنگام مطالعه به دلیل موفقیت یا شکست آشکار انجام میشود.
کاربرد:
- جلوگیری از ادامه مطالعههای بیفایده
- تسریع ورود داروهای مؤثر به بازار
طراحی تطبیقی، ابزار قدرتمندی برای بهینهسازی مطالعات بالینی است. انتخاب نوع مناسب طراحی بسته به هدف مطالعه، مرحله توسعه دارو، نوع بیماری و جمعیت هدف باید با دقت صورت گیرد. با وجود پیچیدگیهای آماری و نظارتی، مزایای این رویکرد مانند افزایش کارایی، کاهش زمان و بهبود نتایج بیماران، آن را به یکی از مهمترین ابزارهای آیندهنگرانه در تحقیقات بالینی تبدیل کرده است.